Propiedades físicas
El agua tiene varias propiedades físicas importantes. Aunque estas propiedades son familiares debido a la omnipresencia del agua, la mayoría de las propiedades físicas del agua son bastante atípicas. Dada la baja masa molar de sus moléculas constituyentes, el agua tiene valores inusualmente grandes de viscosidad, tensión superficial, calor de vaporización y entropía de vaporización, todo lo cual puede atribuirse a las extensas interacciones de enlaces de hidrógeno presentes en el agua líquida. La estructura abierta del hielo que permite la unión máxima de hidrógeno explica por qué el agua sólida es menos densa que el agua líquida, una situación altamente inusual entre las sustancias comunes.
| Propiedades físicas seleccionadas del agua. | |
|---|---|
| masa molar | 18.0151 gramos por mol |
| punto de fusion | 0.00 ° C |
| punto de ebullición | 100.00 ° C |
| densidad máxima (a 3.98 ° C) | 1.0000 gramos por centímetro cúbico |
| densidad (25 ° C) | 0.99701 gramos por centímetro cúbico |
| presión de vapor (25 ° C) | 23.75 torr |
| calor de fusión (0 ° C) | 6.010 kilojulios por mol |
| calor de vaporización (100 ° C) | 40,65 kilojulios por mol |
| calor de formación (25 ° C) | −285.85 kilojulios por mol |
| entropía de vaporización (25 ° C) | 118.8 julios por ° C mol |
| viscosidad | 0.8903 centipoise |
| tensión superficial (25 ° C) | 71,97 dinas por centímetro |
Propiedades químicas
Reacciones ácido-base
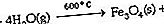
El agua sufre varios tipos de reacciones químicas. Una de las propiedades químicas más importantes del agua es su capacidad de comportarse como ácido (donante de protones) y como base (aceptor de protones), la propiedad característica de las sustancias anfóteras. Este comportamiento se ve más claramente en la autoionización del agua: H 2 O (l) + H 2 O (l) ⇌ H 3 O + (aq) + OH - (aq), donde el (l) representa el estado líquido, el (aq) indica que las especies se disuelven en agua, y las flechas dobles indican que la reacción puede ocurrir en cualquier dirección y existe una condición de equilibrio. A 25 ° C (77 ° F) la concentración de H + hidratado (es decir, H 3 O +, conocido como ion hidronio) en agua es 1.0 × 10 −7 M, donde M representa moles por litro. Como se produce un ion OH - por cada ion H 3 O +, la concentración de OH - a 25 ° C también es 1.0 × 10 −7 M. En agua a 25 ° C, la concentración de H 3 O + y la concentración de OH - siempre debe ser 1.0 × 10 −14: [H +] [OH -] = 1.0 × 10 −14, donde [H +] representa la concentración de iones H + hidratados en moles por litro y [OH -] representa la concentración de OH - iones en moles por litro.
Cuando un ácido (una sustancia que puede producir iones H +) se disuelve en agua, tanto el ácido como el agua contribuyen con iones H + a la solución. Esto lleva a una situación en la que la concentración de H + es mayor que 1.0 × 10 −7 M. Como siempre debe ser cierto que [H +] [OH -] = 1.0 × 10 −14 a 25 ° C, el [OH -] debe bajarse a un valor inferior a 1.0 × 10 −7. El mecanismo para reducir la concentración de OH - involucra la reacción H + + OH - → H 2 O, que ocurre en la medida necesaria para restaurar el producto de [H +] y [OH -] a 1.0 × 10 −14 M. Por lo tanto, cuando se agrega un ácido al agua, la solución resultante contiene más H + que OH -; es decir, [H +]> [OH -]. Dicha solución (en la que [H +]> [OH -]) se dice que es ácida.
El método más común para especificar la acidez de una solución es su pH, que se define en términos de la concentración de iones de hidrógeno: pH = −log [H +], donde el símbolo log representa un logaritmo de base 10. En agua pura, en la que [H +] = 1.0 × 10 −7 M, el pH = 7.0. Para una solución ácida, el pH es inferior a 7. Cuando una base (una sustancia que se comporta como un aceptor de protones) se disuelve en agua, la concentración de H + disminuye para que [OH -]> [H +]. Una solución básica se caracteriza por tener un pH> 7. En resumen, en soluciones acuosas a 25 ° C:
| solución neutral | [H +] = [OH -] | pH = 7 |
| solución ácida | [H +]> [OH -] | pH <7 |
| solución básica | [OH -]> [H +] | pH> 7 |