Gas noble, cualquiera de los siete elementos químicos que forman el Grupo 18 (VIIIa) de la tabla periódica. Los elementos son helio (He), neón (Ne), argón (Ar), criptón (Kr), xenón (Xe), radón (Rn) y oganesson (Og). Los gases nobles son gases incoloros, inodoros, insípidos, no inflamables. Tradicionalmente han sido etiquetados como Grupo 0 en la tabla periódica porque durante décadas después de su descubrimiento se creía que no podían unirse a otros átomos; es decir, que sus átomos no podrían combinarse con los de otros elementos para formar compuestos químicos. Sus estructuras electrónicas y el hallazgo de que algunos de ellos realmente forman compuestos ha llevado a la designación más apropiada, Grupo 18.
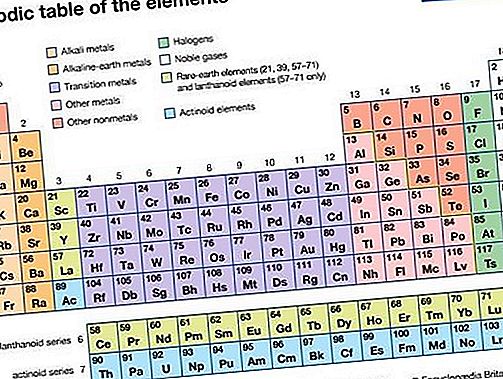
Cuando se descubrieron e identificaron a los miembros del grupo, se pensó que eran extremadamente raros, así como químicamente inertes y, por lo tanto, se los denominó gases raros o inertes. Sin embargo, ahora se sabe que varios de estos elementos son bastante abundantes en la Tierra y en el resto del universo, por lo que la designación rara es engañosa. Del mismo modo, el uso del término inerte tiene el inconveniente de que connota pasividad química, lo que sugiere que no se pueden formar compuestos del Grupo 18. En química y alquimia, la palabra noble ha significado durante mucho tiempo la renuencia de los metales, como el oro y el platino, a sufrir reacciones químicas; se aplica en el mismo sentido al grupo de gases cubiertos aquí.
La abundancia de los gases nobles disminuye a medida que aumenta su número atómico. El helio es el elemento más abundante en el universo, excepto el hidrógeno. Todos los gases nobles están presentes en la atmósfera de la Tierra y, a excepción del helio y el radón, su principal fuente comercial es el aire, del cual se obtienen por licuefacción y destilación fraccionada. La mayor parte del helio se produce comercialmente a partir de ciertos pozos de gas natural. El radón generalmente se aísla como producto de la descomposición radiactiva de los compuestos de radio. Los núcleos de los átomos de radio se descomponen espontáneamente al emitir energía y partículas, núcleos de helio (partículas alfa) y átomos de radón. Algunas propiedades de los gases nobles se enumeran en la tabla.
Algunas propiedades de los gases nobles.
| helio | neón | argón | criptón | xenón | radón | ununoctium | |
|---|---|---|---|---|---|---|---|
| * A 25.05 atmósferas. | |||||||
| ** hcp = hexagonal compacto, fcc = cúbico centrado en la cara (cúbico cerrado). | |||||||
| *** El isótopo más estable. | |||||||
| número atómico | 2 | 10 | 18 años | 36 | 54 | 86 | 118 |
| peso atomico | 4.003 | 20,18 | 39,948 | 83,8 | 131,293 | 222 | 294 *** |
| punto de fusión (° C) | −272.2 * | −248.59 | −189.3 | −157.36 | −111.7 | −71 | - |
| punto de ebullición (° C) | −268,93 | −246.08 | −185.8 | −153,22 | −108 | −61,7 | - |
| densidad a 0 ° C, 1 atmósfera (gramos por litro) | 0.17847 | 0.899 | 1.784 | 3.75 | 5.881 | 9,73 | - |
| solubilidad en agua a 20 ° C (centímetros cúbicos de gas por 1,000 gramos de agua) | 8.61 | 10,5 | 33,6 | 59,4 | 108,1 | 230 | - |
| abundancia isotópica (terrestre, porcentaje) | 3 (0.000137), 4 (99.999863) | 20 (90,48), 21 (0,27), 22 (9,25) | 36 (0,3365), 40 (99,6003) | 78 (0,35), 80 (2,28), 82 (11,58), 83 (11,49), 84 (57), 86 (17,3) | 124 (0,09), 126 (0,09), 128 (1,92), 129 (26,44), 130 (4,08), 131 (21,18), 132 (26,89), 134 (10,44), 136 (8,87) | - | - |
| isótopos radiactivos (números de masa) | 5–10 | 16-19, 23-34 | 30–35, 37, 39, 41–53 | 69–77, 79, 81, 85, 87–100 | 110–125, 127, 133, 135–147 | 195–228 | 294 |
| color de la luz emitida por el tubo de descarga gaseosa | amarillo | rojo | rojo o azul | amarillo verde | azul a verde | - | - |
| calor de fusión (kilojulios por mol) | 0,02 | 0,34 | 1,18 | 1,64 | 2.3 | 3 | - |
| calor de vaporización (calorías por mol) | 0,083 | 1,75 | 6.5 | 9.02 | 12,64 | 17 | - |
| calor específico (julios por gramo Kelvin) | 5.1931 | 1.03 | 0.52033 | 0.24805 | 0.15832 | 0,09365 | - |
| temperatura crítica (K) | 5.19 | 44,4 | 150,87 | 209,41 | 289,77 | 377 | - |
| presión crítica (atmósferas) | 2,24 | 27,2 | 48,34 | 54,3 | 57,65 | 62 62 | - |
| densidad crítica (gramos por centímetro cúbico) | 0,0696 | 0,4819 | 0,5356 | 0,9092 | 1.103 | - | - |
| conductividad térmica (vatios por metro Kelvin) | 0,1513 | 0,0491 | 0,0177 | 0.0094 | 0.0057 | 0.0036 | - |
| susceptibilidad magnética (unidades cgs por mol) | −0.0000019 | −0.0000072 | −0.0000194 | −0.000028 | −0.000043 | - | - |
| estructura cristalina** | hcp | fcc | fcc | fcc | fcc | fcc | - |
| radio: atómico (angstroms) | 0,31 | 0,38 | 0,71 | 0,88 | 1.08 | 1,2 | - |
| radio: covalente (cristal) estimado (angstroms) | 0,32 | 0,69 | 0,97 | 1.1 | 1.3 | 1,45 | - |
| polarización estática (angstroms cúbicos) | 0,204 | 0,392 | 1,63 | 2.465 | 4.01 | - | - |
| potencial de ionización (primero, electronvoltios) | 24.587 | 21.565 | 15,759 | 13,999 | 12.129 | 10.747 | - |
| electronegatividad (Pauling) | 4.5 4.5 | 4.0 4.0 | 2.9 | 2.6 | 2,25 | 2,0 | - |






![Batalla de la historia francesa de Rocroi [1643] Batalla de la historia francesa de Rocroi [1643]](https://images.thetopknowledge.com/img/world-history/6/battle-rocroi-french-history-1643.jpg)